線維筋痛症のメカニズム
まとめ:線維筋痛症のメカニズムは、中枢感作(脳や脊髄で痛みに対して過敏になる)と説明されて中枢性鎮痛剤が治療薬として掲げられています。一方で、中枢だけでなく末梢性の変化や抗体の関与も示唆されています。これを末梢感作と言います。
線維筋痛症やその他の慢性重複疼痛疾患は、歴史的に「末梢」疼痛理論に基づく説明が困難でしたが、現在ではこれらの疾患は中枢神経系因子の重大な変化によって疼痛と感覚処理が増強されることが明らかになっています。線維筋痛症を模倣した動物モデルでは、脊髄から皮質までの中枢神経系の変化が発見されました。(2016, Slika)
FMSの患者で、神経炎症(髄液で評価)と慢性全身性炎症(血漿で評価)の両方の証拠が見つかりました。患者と対照群を高度に識別する2つのタンパク質群(髄液用と血漿用)が提示されました。特に、髄液ケモカインCX3CL1(フラクタルカインとしても知られる)の高濃度が認められました。さらに、FMにおけるIL-8に関する過去の知見が、髄液と血漿の両方で再現されました。(2017, Bäckryd)
線維筋痛症(FMS)の中心にある現象として、中枢感作がfMRIの研究によって2002年に証明され(2002, Gracely)、FMSは単なる精神疾患ではないことが明らかにされました。中枢感作とは、FMSでは痛み閾値の低下がありますが、これは「痛みの信号が中枢で増幅されたまま戻らない状態」のことです。(2006, Staud)
FM患者が、覚醒時および睡眠時の慢性疼痛の強さに起因する交感神経の過剰活動と一致する自律神経系の機能不全を有することを裏付けています。(Rizzi, 2017)睡眠中も交感神経優位な闘争・逃走反応が起こっています。
線維筋痛症患者の筋肉間質結合組織では、対照群と比較してAGE(終末糖化産物) CMLの染色がより強く、NF-κBが活性化し、血清中のCMLレベルも高かった。RAGEはFM筋にのみ存在した。タンパク質のAGE修飾は、変性タンパク質(例:AGE修飾コラーゲン)の溶解性低下とタンパク質分解に対する高い抵抗性を引き起こす。AGEは、細胞表面のAGE特異的受容体(例:RAGE)を介して転写因子NF-κBを活性化することで、様々な細胞を刺激する。これらのメカニズムはいずれも、FM患者に特徴的な疼痛の発現、持続、および拡大に寄与している可能性がある。(2005, Rüster)
運動介入前後の外側広筋における鎮痛剤および代謝物の組織内濃度を調べた。FMSは、グルタミン酸、ピルビン酸、乳酸の組織間濃度の有意な上昇と関連していました。運動介入後、FMS群では疼痛強度とグルタミン酸、ピルビン酸、グルコースの平均組織間濃度が有意に低下しました。FMSにおける疼痛強度の低下は、ピルビン酸およびグルコースの減少と有意に相関していました。さらに、FMS群では筋力と持久力が向上しました。FMS患者において末梢代謝および鎮痛筋の変化が存在し、これらの変化が疼痛に寄与しているという示唆を裏付けています。運動介入後、これらの変化は正常化し、疼痛強度は低下しましたが(消失したわけではありません)、筋力と持久力は改善しました。これらの所見はすべて、運動の効果が部分的に末梢的であることを示唆しています。(2010, Gerdie)
FMS患者の僧帽筋圧は著しく上昇しており、これはFMSの本質的な特徴である可能性があり、診断評価の一環としてモニタリングできる可能性がある。圧異常による負担は、FMSのびまん性筋痛を説明する一助となる可能性がある。したがって、FMSを中枢性疼痛処理障害として再考する必要がある。治療的には、筋圧の軽減が臨床像を大きく変化させる可能性がある。(2021, Katz)
線維筋痛症(FM)患者における表面筋電図(SEMG)反応を調査したところ、FM患者は健常者と比較して、SEMG信号の中央スペクトル周波数(MDF)および伝導速度(CV)の初期値と変化率に関して興味深い筋変化が認められました。FM患者ではこれらの値が有意に低下していました。患者は筋線維の動員方法が異なるか、あるいはII型線維の萎縮がみられる可能性があり、これが筋弛緩を達成できないことを示唆しています。(2009, Bazzichi)
線維筋痛症の病態を標的とする従来の治療法は効果が限られています。それらは主に薬理学的な性質を保っており、患者が訴える様々な疾患の症状面を治療する傾向があります。しかしながら、統計によると、線維筋痛症患者の90%が症状の管理に補完医療も利用しているという事実が浮き彫りになっています。(2021, Siracusa)
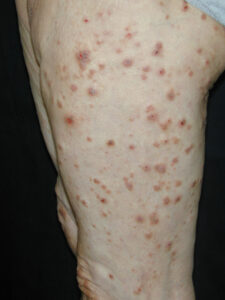
線維筋痛症では、小線維神経障害(small fibers neuropathy)とは「脳と脊髄の外側」にある末梢神経の障害がある。小線維(C線維・Aδ線維・自律神経線維) が損傷している。(皮膚生検で確認)多様な症状を起こすため診断が難しい。例えると「盲人と象」で、患者ごとに見える症状がバラバラになる。免疫グロブリン療法に反応する可能性があります。(2018, Martínez-Lavín)
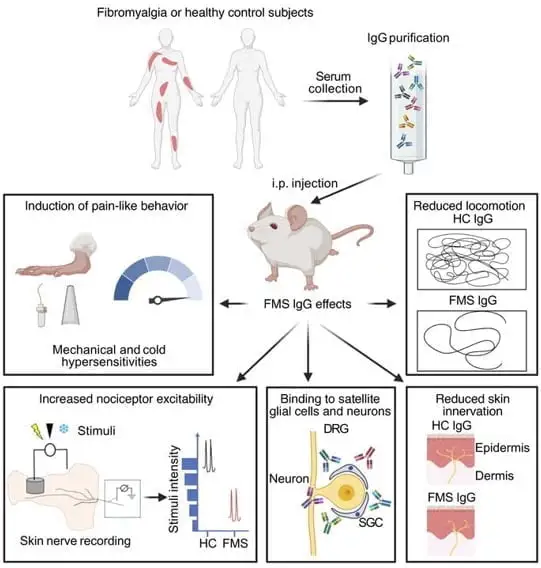
FMS患者由来のIgGが侵害受容ニューロンを感作することで感覚過敏症を引き起こすことを示します。FMS患者由来のIgGを投与したマウスは、有害な機械的刺激と冷感刺激に対する感受性の増加を示し、FMS IgGを投与したマウスの皮膚神経標本中の侵害受容線維は、冷感と機械的刺激に対する反応性の増加を示しました。これらのマウスは、自発運動の低下、肢の握力の低下、および表皮内神経支配の喪失も示しました。本研究の結果は、FMS患者由来のIgGが末梢痛覚求心性神経を感作することで疼痛感覚過敏を引き起こすことを実証し、患者のIgG抗体価を低下させる治療法が線維筋痛症に有効である可能性を示唆している。このマウスのFMS症状は一過性で、IgG抗体が消失すれば同時に見られなくなりました。(2021, Goebel)ただし、FMSの病態は抗体だけでは説明できません。他の自己免疫疾患のようにステロイドが有効ではありません。
線維筋痛症は、感染症およびワクチン接種後に発症することが知られています。FMの半数は感冒後に発症します。また、ライム病、マイコプラズマ、C型肝炎、およびHIV感染後に発症した症例が詳述されている。湾岸戦争症候群は、線維筋痛症と多くの臨床的特徴を共有する機能的多系統疾患であり、ペルシャ湾派遣中の複数回のワクチン接種とストレスおよび外傷との相互作用との関連が指摘されています。(2006, Ablin)(2006, 松本)
脳脊髄液中に発痛物質として知られているサブスタンスPが増加し、下降性疼痛抑制系の中心と考えられているセロトニン前駆体やその代謝物の減少が指摘され、疼痛に関する情報伝達の異常が線維筋痛症の原因と考えられている。(Yunus, 2007)(Russell, 1994)
若年性線維筋痛症の診断については、2010年に撤廃された特徴的圧痛点の存在が中核症状と考えられる。また、参考症状として、低体温、IBS、天候による影響があり、性格特徴として、いわゆる“良い子”、完全主義、固執傾向、非妥協的、コミュニュケーション障害、他人への過剰な気遣い(過剰適応)があります。とくに小児例では,母子の関わり方に問題がある例がみられる.典型例では,10才までの性格形成期に,母親に甘えたいときに甘えられる状況が適えられなかったことで,いわゆる “甘え下手”で自己認識,自己表現が乏しく,周囲とのコミュニケーションが上手に確立できない症例が目立つことが報告されています。(2014、宮前)