筋萎縮性側索硬化症
筋萎縮性側索硬化症(ALS、amyotrophic lateral sclerosis)は、1869年に、フランスの脳神経内科医のシャルコー(1825~1893)によって初めて報告された疾患です。上位運動ニューロンと下位運動ニューロンの両者の細胞体が散発性・進行性に変性脱落する神経変性疾患です。
■環境毒素によるリスク
筋萎縮性側索硬化症のクラスターが、南フランスの沿岸地区であるエロー地区(2013、Maserret)やニューハンプシャー州エンフィールド(2009, Caller)などで特定されています。シアノバクテリア由来の神経毒であるベータ-N-メチルアミノ-L-アラニン(BMAA)の潜在的な食事源からの暴露が想定されています。
筋萎縮性側索硬化症との122種類の環境毒素との関連を調べた研究で、農薬と兵役に関係する残留性環境汚染物質の血中濃度との相関を認めました。(2016年、Suら)
■新型コロナウイルスおよびワクチン接種との関連
新型コロナウイルス感染によって症状が加速したALSの患者が報告されています。(2021, Li)
新型コロナワクチン接種5日後に、運動障害とMRIの異常(皮質脊髄路のワーラー変性、ALSやアルツハイマー病などの神経変性疾患で見られる所見)が出現した症例が報告されています。(2022, Ghosh)
■ミトコンドリア障害に対する適応反応として起こる高脂血症
ALS患者は、代謝亢進や脂肪酸代謝の変化、高脂血症、体重減少の代謝表現型の変化を示すことが一般的で、これらは生存期間と相関しています。(2011, Dupuis)
高脂血症に関するデータは一貫しており、逆説的でもあります。高脂血症とそれに対応するより高いBMIの両方が疾患の進行を保護すると報告されています。(2008年、Dupuis)(2018、Dardiotis)
ケトジェニックダイエットのALSに対する有効性が報告されています。これはケトン体が、抗酸化特性による神経保護作用と、運動ニューロンにおけるグルコースの代替供給源となると考察されています。(2020年、Caplliure‐Llopis)
糖尿病と筋萎縮性側索硬化症 (ALS) の関係に関する研究では、相反する結果が得られています。若い患者では、糖尿病は ALS の一貫した危険因子です。高齢患者では、糖尿病はヨーロッパでは ALS を予防しますが、アジアでは ALS のリスクを高めます。(2015年、Logrosino)
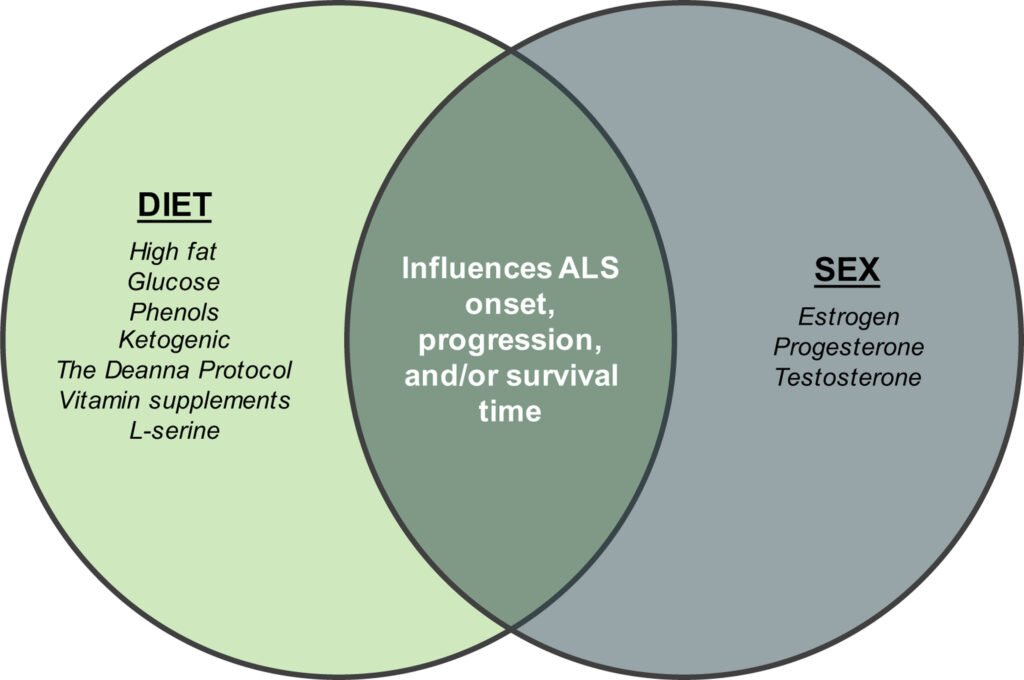
■体重を増やす食事(高脂肪、高糖、高カロリー食)の保護効果
体重を増やす食事(高脂肪、高糖、高カロリーの食事)は、代謝亢進と病気の進行による栄養失調と戦うことによる保護作用が示されています。
高カロリー脂肪食がALSの急性期において進行を遅らせることが報告されています。(2020, Ludruph)
ALSの線虫モデルで、メープルシロップ(スクロースとフェノールを多く含む)が保護作用があることが報告されています。(2016, Aaron)
ALSのマウスモデルで、アルギニン-アルファ-ケトグルタル酸と高脂肪食のケトジェニック ダイエットが保護作用があることが報告されています。(2014, Ari)
■ROS産生を減少させる可能性のある抗酸化効果を持つフィトケミカル
野菜や果物を摂取することでALSのリスクが低下することが、日本(2009, Okamoto)や韓国(Jin, 2014)から報告されています。
ALSの動物モデルで、イチゴ由来のアントシアニンの保護効果が報告されています。(2018, Winter)
■性差
ほとんどの研究では、男女比 3:2 で男性が優勢であることを示しています。(2012, Blasco)
性ホルモンは食事とは無関係に ALS において重要な役割を果たし、女性は ALS の発症、疾患の重症度、および疾患の進行から保護されることが考察されています。(2020年、Papeら)