キレーション点滴とオリゴスキャン
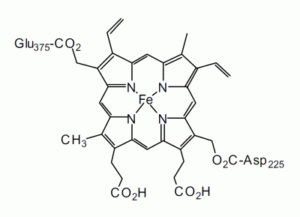
EDTAは、4つのカルボキシル基(-COOH)と2つのアミン基(-NH-)を持つ分子で、これらが金属イオンと配位結合を形成します。この多座配位子としての性質により、EDTAは金属イオンを「包み込む」ように結合し、安定なキレート錯体を形成します。このキレート効果が、EDTAの高い親和性の鍵です。
EDTAの金属イオンに対する親和性は、**安定定数(K)**で表されます。安定定数は、錯体がどれだけ安定かを示す指標で、数値が大きいほど親和性が強いことを意味します。以下に代表的な金属イオンとEDTAの安定定数(log K)の例を示します。
1価金属イオンは、EDTAが得意とする多価金属イオン(例: Fe³⁺, Cu²⁺, Al³⁺など)とは異なり、キレート錯体を形成する条件を満たさないか、親和性が極めて低いです。EDTAの安定定数は、主に2価以上の金属イオンに対して意味を持ちます。
| カルシウム | Ca²⁺ | 10.7 | アルミニウム | Al³⁺ | 16.1 |
| マグネシウム | Mg²⁺ | 8.7 | アンチモン | 錯体形成は弱い | |
| リン | 錯体形成せず | 銀 | Ag⁺ | 7.32 | |
| ケイ素 | 錯体形成せず | ヒ素 | 錯体形成せず | ||
| ナトリウム | log K ≈ 1.7 | バリウム | Ba²⁺ | 7.76 | |
| カリウム | K⁺ | log K < 1(ほぼ錯体形成せず) | ベリリウム | Be²⁺ | 9.7 |
| 銅 | Cu²⁺ | 18.8 | ビスマス | Bi³⁺ | 27.94 |
| 亜鉛 | Zn²⁺ | 16.5 | カドミウム | Cd²⁺ | 16.5 |
| 鉄 | Fe²⁺(Fe³⁺) | 14.3(25.1) | 水銀 | Hg²⁺ | 21.5 |
| マンガン | Mn²⁺ | 13.9 | ニッケル | Ni²⁺ | 18.62 |
| クロム | Cr³⁺ | 23.4 | プラチナ | Pt²⁺ | 20(推定) |
| パナジウム | V²⁺(V³⁺) | 12.7(18) | 鉛 | Pb²⁺ | 18 |
| ホウ素 | 錯体形成せず | タリウム | Tl⁺ | 6.54 | |
| コバルト | Co²⁺ | 16.45 | トリウム | Th⁴⁺ | 23.2 |
| モリブデン | 錯体形成は弱い | ガドリニウム | Gd³⁺ | 17.37 | |
| ヨウ素 | 錯体形成せず | 鈴 | Sn²⁺ | 18.3 | |
| リチウム | Li⁺ | log K < 1(ほぼ錯体形成せず) | |||
| ゲルマニウム | データなし | ||||
| セレン | 錯体形成せず | ||||
| 硫黄 | 錯体形成せず | ||||
| フッ素 | 錯体形成せず |
■EDTA製剤の使い分け
| NaEDTA | 動脈硬化治療(血管内のカルシウム沈着を除去)+重金属デトックス |
| NaCaEDTA | 重金属デトックス、特に鉛中毒に使われます |
| MgEDTA | 動脈硬化治療+重金属デトックス+Mg補給、製造が難しく高価 |
■キレーション治療の問題点
安定定数の高い必須ミネラルの銅、亜鉛、鉄、マンガン、クロム、パナジウム、コバルトがキレートされてしまうので、補給する必要があります。
血中に存在する多価金属イオンを除去しますが、筋肉や骨など血中外の金属イオンは除去出来ません。
| 骨 | 筋肉 | 内蔵 | 血液 | |
| アルミニウム | 50~60% | 10〜20% | 10〜20% | 1%以下 |
| 水銀 | 5~10% | 20〜30% | 60~70% | 1~5% |
| カドミウム | 10〜20% | 5〜10% | 70〜80% | 1%以下 |
| 鉛 | 90〜95% | 1〜2% | 2~5% | 1~5% |
| 元素 | 主な半減期 | 主な蓄積部位 | 排泄経路 |
| アルミニウム | 数時間〜数ヶ月 | 骨、脳、肺 | 尿 |
| 水銀 | 40〜70日 | 脳、腎臓、血液 | 尿、便、毛髪 |
| カドミウム | 10〜30年 | 腎臓、肝臓 | 尿(非常に遅い) |
| 鉛 | 血液: 30日、骨: 10〜30年 | 骨、血液、軟組織 | 尿、便 |
■その他
pH: EDTAのカルボキシル基はプロトン化(-COOH)または脱プロトン化(-COO⁻)の状態に依存します。pHが高いほど脱プロトン化が進み、金属イオンとの結合が強まります。通常、pH 4~10の範囲で効果を発揮します。点滴に炭酸水素ナトリウム 10ml~20mlを追加します。炭酸水素ナトリウムはpHを上げます。EDTAは4つのコーナーを持つ分子でこれ等全てが(-)チャージであると(+)チャージの重金属を捕獲しやすいので、血液がよりアルカリ性である事が解毒には重要です。
金属イオンの電荷とサイズ: 電荷が大きく、イオン半径が適度な金属イオン(例: Fe³⁺)ほど親和性が高くなります。
競合する配位子: 溶液中に他のキレート剤や配位子(例: リン酸イオン、硫酸イオン)がある場合、EDTAの親和性が競合により低下することがあります。
■EDTAサプリメント
市販されているEDTAサプリは、NaCaEDTAです。必須ミネラルのMgが優先的にキレートされて排出されますので、同時にMgの摂取が必要です。