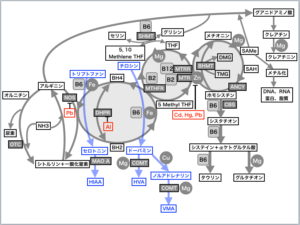
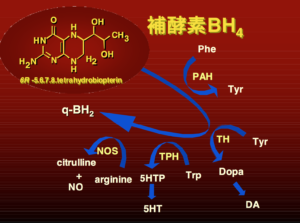
カドミウム(Cd)
四大公害のひとつであるイタイイタイ病は、カドミウムの蓄積が原因です。
カドミウムの生物学的半減期は一般に16~38年ぐらいと言われています。
生体に吸収されて肝臓に入ったカドミウムは、そこで有害金属から身体を守るタンパク質であるメタロチオネインとなり、腎臓にまで運ばれ、腎臓皮質にある程度まで蓄積されます。メタロチオネインは、金属と容易に結合するタンパク質で、金属元素を無機塩の型で経口的に摂取した場合に、金属元素と親和性の強いタンパク質が誘発的に生合成され、金属イオンとタンパク質からなる有機金属化合物となります。それが生体の毒物などに対する制御作用物質として働くために、カドミウムや亜鉛・銅・水銀はある程度まで体内に蓄積されてしまいます。
体内のカドミウムは、肝臓と腎臓に50-70%存在します。
腎臓中のカドミウム濃度が過剰になり、メタロチオネインのSH基と結合できないカドミウムが出現すると、それによって腎臓の障害が発症します。
この腎臓へのカドミウムの蓄積によって、近位尿細管障害にはじまる腎機能障害を起こし、重症例では腎不全になります。
ビタミンDの活性化は腎臓で行いますが、カドミウムよる腎障害のために、ビタミンDの活性化が出来ないために、骨粗鬆症となって骨が折れやすくなります。
イタイイタイ病でのカドミウムの侵入経路は、米と言われています。
土壌中のカドミウム濃度と玄米中カドミウム濃度の間には相関関係が認められず、土壌中のカドミウム含量が低くても、高濃度の汚染米が出現することが知られています。
なお、精製米は玄米と同等のカドミウムを含んでいることが報告されています。
カドミウムの侵入経路としては、他にタバコ、大気汚染があります。
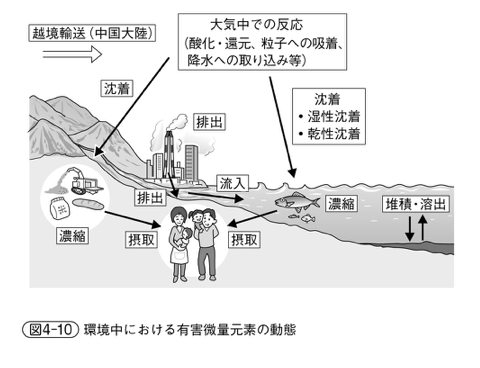
検査は、尿中カドミウム(0.5μg/dL以下)、尿中β2マイクログログリン(289μg/L以下)があります。
一般的には、前者は急性中毒、後者は慢性中毒の指標です。つまり腎障害は不可逆です。
下記は、当時の検査結果ですが、全国的に尿中のカドミウムが検出されています。
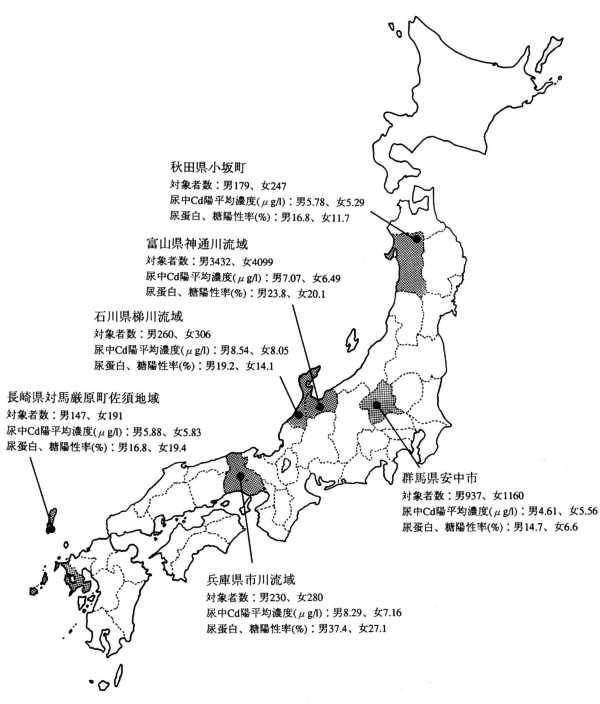
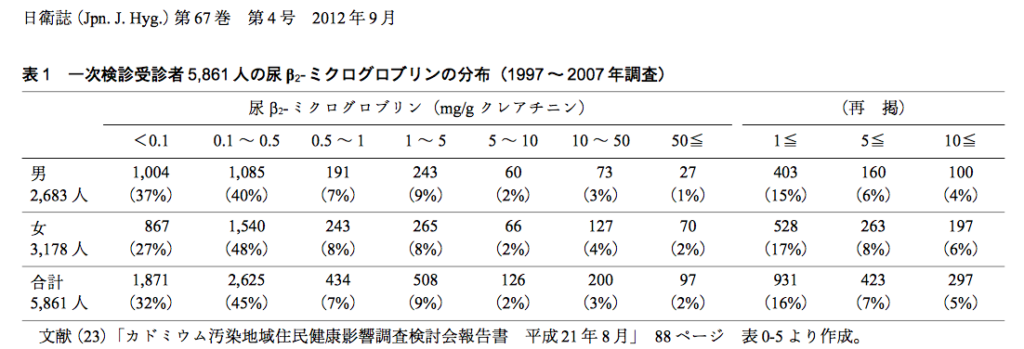
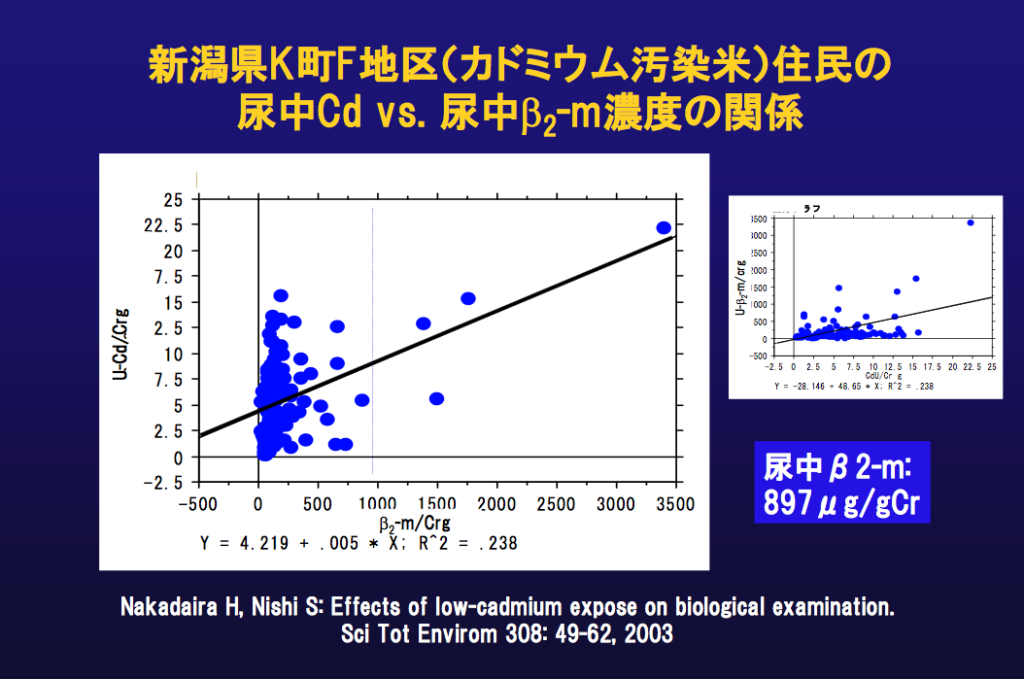
近位尿細管障害を見るために尿中α1マイクログログリンの測定や、尿蛋白・尿糖の定性を簡易的に見る方法もあります。
DMSAを服用後に尿経路誘発有害金属ミネラル検査を行う方法もあります。
国内のカドミウムの汚染状況を示す地球化学図が公表されています。