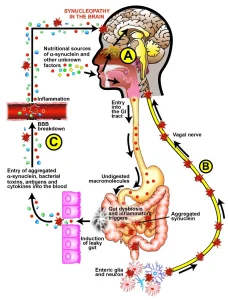
パーキンソン病の栄養療法
まとめ:パーキンソン病の栄養療法は、第一にGFCFを行って、第二に野菜・果物を積極的に摂取して快便を目指すことが大切です。
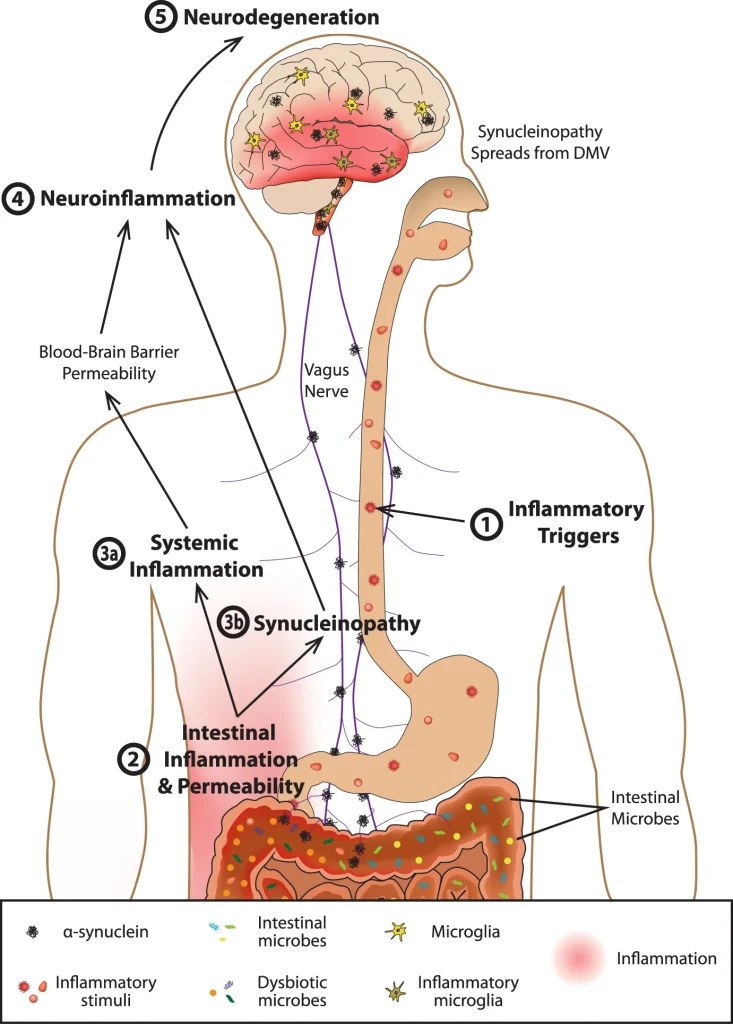
パーキンソン病が便秘から始まり、腸にダメージを与えて便秘にさせる食物が根本原因のひとつであることが指摘されています。(2020年のChaoら、2021年のVojdaniら)
便秘や下痢などの消化器症状は小麦製品と乳製品に含まれるグルテンとカゼインが、体内でオピオイド様ペプチドに代謝されて、これが消化管を麻痺させることが根本原因です。
従って、まず第一にグルテンフリー・カゼインフリーダイエット(GFCF)を行って、便秘を治すことが先決です。
パーキンソン病に対するGFCFはこれまでにランダム化比較試験が行われておらず、症例報告でのみ有効性が報告されています。(2014年、Lazzaroら)
乳製品を摂取するとパーキンソン病のリスクが上がることが報告されています。(2014年のJiangら、2017年のHughesら)
GFCFを行っても便秘が治らない場合は、食物繊維が不足しています。食物繊維の推奨量は1日700gと大量ですから、簡単には摂取出来ません。にんじんジュースなどを使えば、便秘の解消に役立ちます。
まずGFCFを実践して根本原因を解決してから、次に野菜・果物で食物繊維を摂取する順番で、便秘を解消することを勧めます。
パーキンソン病の治療にプレ・プロバイオティクスが推奨されていますが(2017年のPerez-Pardoら、2016年のBarichellaら)、前駆体の野菜・果物を摂取する方が有益です。
パーキンソン病に対して地中海式ダイエットの有効性が報告されています(2009年のBarichellaら、2012年、Alcalayら)が、毎日野菜と果物を摂取して便秘を解消するという話に繋がります。
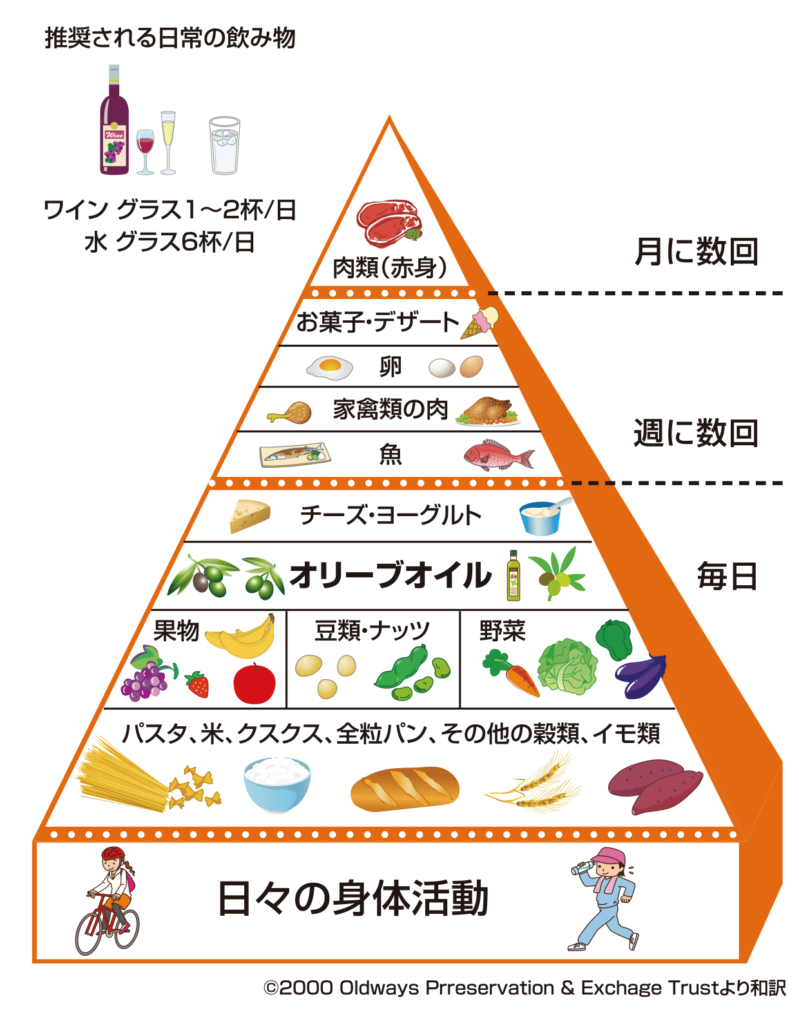
2020年にMobDisordは、パーキンソン病の栄養療法に関する総論を出しており、ビタミンB、ビタミンD、亜鉛の不足と補給による有効性が指摘されています。
パーキンソン病のハエモデルではビタミンCが用量依存性に効果があることが報告されています。(2019, Man Anh)
メタアナリシスにて、パーキンソン病に対するビタミンCとβカロチンの保護効果は認められませんでしたが、ビタミンEの保護効果が認められました。(2005, Etminan)
in vitro で動物モデルを使用して実施された研究の増加は、パーキンソン病の食事による予防における潜在的な役割を示していますが、ヒトでそうするための栄養介入の有効性は依然として議論の余地があります。抗酸化微量栄養素の食事摂取とパーキンソン病発症のリスクを調べる疫学的研究では、あいまいな結果が得られており、既存のパーキンソン病患者を対象としたランダム化比較試験のデータは不足しています。食事の抗酸化物質は、単一の特定のプロセスを標的にするのではなく、複数の効果を発揮します。ビタミン C、ビタミン E、およびポリフェノールは ROS と直接相互作用し、酸化連鎖反応を停止します。セレンのような他のミネラルは、抗酸化酵素の活性をサポートする補因子として機能します. 多くの抗酸化栄養素がシグナル伝達に関与し、酸化ストレスの下流の標的を保護して、パーキンソン病の発症を促進する損傷を緩和します。栄養素は、ドーパミン作動性ニューロンの発生、成長、および生存を制御する遺伝子も調節します。クルクミン、レスベラトロール、カテキン、オレウロペインなどのポリフェノールは、レビー小体の形成を阻害します。(2020, Park)
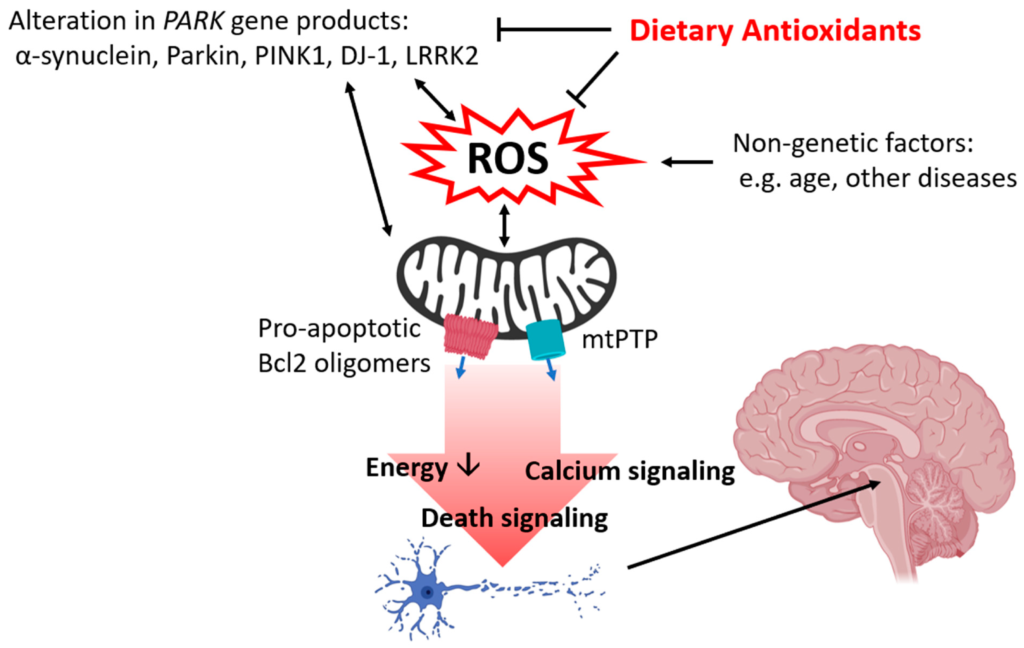
2019年にBoulosらは、パーキンソン病の栄養療法に関する総論を出しており、尿酸、コーヒー、お茶が保護効果を持つこと、乳製品がリスクがあることを総括しています。
毎日20gのホエイプロテインを補給すると、運動機能が改善され、炎症に関連するホモシステインが減少し、血漿中の還元型グルタチオンが大幅に増加し、パーキンソン病患者の解毒に必要なグルタチオン合成が増加することが報告されています。(2016年、Tosukhowongら)
パーキンソン病では一般にホモシステインが高く、ビタミンBの投与で低下することが報告されています。(2016年のIbrahimagicら、2005年のLamberitiら)
ケトジェニックダイエットやグルテンフリーダイエットのような高タンパク食は、パーキンソン病のための有効な介入として提案されています。(2018年のPhillipsら)
パーキンソン病の発症リスクについては、喫煙とコーヒーの飲用の両方が発生率の大幅な低下と関連しており、タバコとコーヒーの保護効果は、少なくとも部分的には微生物叢の調節によって媒介される可能性があることが報告されています。(2014年のDerkindernら、2015年のScheperjansら)
2021年にVojdaniらは、頻繁に摂取される食品は、リーキガット症候群がある場合に、血液に入る可能性があると仮定しました。侵入した食物に対する抗体は、パーキンソン病および他の神経変性障害を有する患者のα-シヌクレイノパチーに寄与する可能性があります。さらに、それらの間の交差反応性が配列類似性と共存する場合、2つの経路はPDにおける自己免疫形成の過程で一緒に結合することができます。循環中のaSN抗体のレベルが上昇している個人では、これらの抗体はaSNを含む食品と反応し、血液脳関門(BBB)を通過して脳に入る免疫複合体を形成し、レビー小体の形成を誘発する可能性を指摘しました。
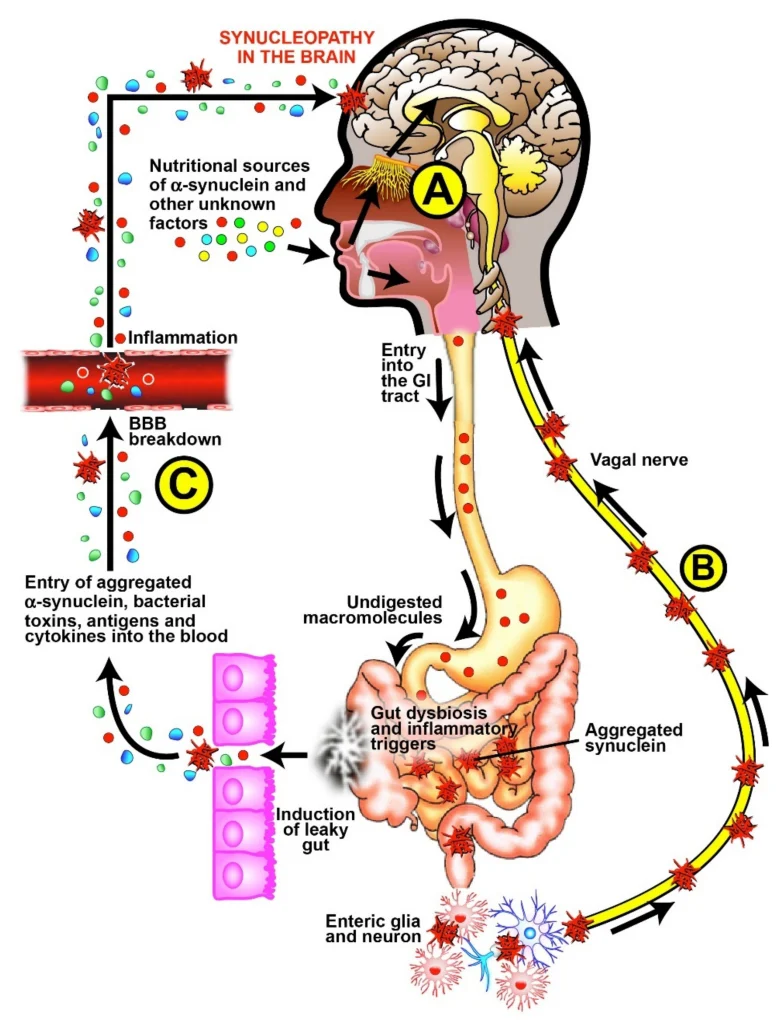
また、α-シヌクレインと交差反応性と配列相同性で問題になる食品タンパク質として、酵母、大豆、ラテックスヘベイン、小麦胚芽凝集素、ジャガイモ、ピーナッツ、豆凝集素、エンドウ豆レクチン、エビ、ブロメラン、レンチルレクチンを指摘しました。
2008年にPetersonらはパーキンソン病の発病リスクと、成人期の鯨肉と脂身の食事摂取量および食費汚染物質(溶剤、農薬、金属への職業的接触)への暴露と関係することを報告しています。
海外で禁止されているパラコートなどの農薬が原因となることが指摘されています。
パーキンソン病の環境リスクを評価したメタアナリシスでは、身体活動と便秘がクラス Iのリスク、頭部外傷、不安またはうつ病、ベータ遮断薬、喫煙、および血清尿酸は、関連性についてクラス IIのリスクとしました。(2016, Bellou)
パーキンソン病では尿酸が低下することが12の論文で指摘されています。(2017, Yu)
パーキンソン病に対する運動介入の有効性が総括されています。(2008, Goodwin)(2019, Xu)