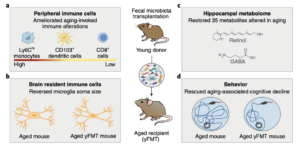
感染後過敏性腸症候群
(2020年6月27日の記事を加筆修正しました。)
過敏性腸症候群(IBS)は、腸に異常がないにも関わらず下痢や便秘や腹部膨満や腹痛などの下腹部不快感を繰り返す慢性疾患ですが、一部のIBSは食あたりや胃腸炎の後に発病することが知られています。
1950年にStewartらは、第二次世界大戦中に北アフリカに進軍したイギリス軍で、急性のアメーバ赤痢に感染した後に、慢性のIBSを発病した34例を初めて報告しました。
その後同様の報告が集積されて、IBSの10%〜35%は、急性の食あたりや胃腸炎の後に、小腸内細菌増殖症(SIBO)が起こり、結果として慢性のIBSが発症することが明らかにされています。
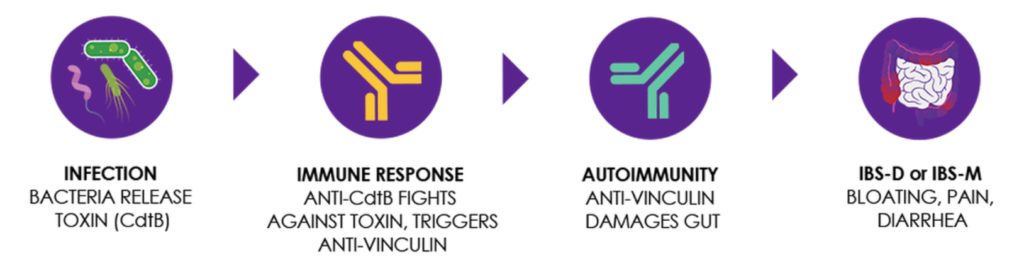
食中毒(カンピロバクター菌、サルモレラ、赤痢菌、病原大腸菌)が起きると、これらの菌は細胞致死毒素B(Cytolethal Distending Toxin B、CbtB)と言われる毒素を腸内で放出します。
人体は異物であるこの毒素に対する抗CbtB抗体を作ります。
この毒素のCbtBは、腸の収縮に関係するビンキュリンタンパク(Vinculin)とよく似ているために(分子模倣、molecular mimicry)、ビンキュリンタンパクに対する抗ビンキュリン抗体も同時に作るようになります。
抗ビンキュリンの産生は自己免疫反応であり、腸神経の損傷とカハール介在細胞(ICC)および遊走運動複合体(MMC)の機能低下につながります。
この抗ビンキュリン抗体が小腸を攻撃するため、小腸の蠕動運動が悪くなり、大腸の細菌が流入してSIBOとなり、その結果としてガスや下痢などを発症するIBSとなります。
腸神経の損傷とカハール介在細胞(ICC)および遊走運動複合体(MMC)が適切に機能しない場合、腸内細菌叢が破壊されます。大腸の腸内細菌叢は、腸内の何十億ものバクテリアで構成されており、バランスが取れていると、腸を健康に保ちます。
原因が不明で症状から診断されるIBSの一部は、自己免疫疾患であることが明らかにされました。
自己抗体を調べることによって、確定診断が出来るようになっています。(2019年、Moralesら)→IBS検査を実施しています。
この感染後過敏性腸症候群は、下痢型または混合型であり、便秘型ではありません。
便秘型の過敏性腸症候群は、発病機序から見ると別の疾患になります。
第1の問題は小腸に存在するので、大腸の治療ではなく、小腸のSIBOの治療を行うことが大事です。
このSIBOの治療は、小腸の動きが悪く逆流が起きていることが原因なので、抗生剤の使用よりも、長期的なSIBO食、自己免疫疾患の栄養療法を継続することがポイントになります。