ME/CFSのメカニズムと治療
まとめ:ME/CFS(筋痛性脳脊髄炎/慢性疲労症候群 )では自己免疫反応による免疫炎症、酸化ストレス、ニトロソ化ストレスが、ミトコンドリアなどでの代謝障害を引き起こしていると考えられます。新型コロナ後遺症、新型コロナワクチン後遺症でも似た病態が起こってくるのではないかと考えています。
ME/CFS 患者では血中ホモシステイン値は常に上昇しているわけではありませんが、脳脊髄液中のホモシステイン値が非常に著しく上昇しており、脳脊髄液ホモシステインレベルは「疲労」の客観的評価と有意に相関することが指摘されています。(1997, Regland)
新型コロナウイルス感染症の重症化やロングコビットでは、血清ホモシステインレベルの上昇との関係が指摘されています。
ME/CFSとロングコビットが似た病態であることが指摘されています。(2021, Wong)
ME/CFSは複数のメタボロミクス解析によって、低代謝症候群であることが指摘されており(2016, Nauviaux)(2018, Tomas)、この低代謝状態の最も一貫した所見は、免疫炎症、酸化ストレス/ニトロソ化ストレス(活性酸素/窒素種 (ROS/RNS) )です。(2014, Morris)
ミトコンドリア損傷の増加、ATP 産生の減少、および酸化的リン酸化の障害はすべて、ME/CFS がミトコンドリア病である可能性を示しています。(2021, Toogood)(2014, Morris)
ME/CFSが一次的なミトコンドリア障害ではないことを示唆する一貫したゲノム研究がありますが、ミトコンドリア機能の低下は、他の経路の破壊による二次的な影響により発生する可能性があります。抗ミトコンドリア抗体も検出されていません。(2020, Holden)
筋痛性脳脊髄炎/慢性疲労症候群 (ME/CFS) では、β2アドレナリン受容体(β2AdR)およびM3アセチルコリン受容体抗体の上昇が見られました。β2AdR と M3 アセチルコリン受容体は両方とも重要な血管拡張剤であるため、それらの機能障害が血管収縮と低酸素血症を引き起こすと予想されます。循環と酸素供給の障害は、ME/CFS の多くの症状を引き起こす可能性があります。(2020, Wirth)(2021, Wirth)
アドレナリン作動性/ムスカリン受容体に対する自己抗体が、筋痛性脳脊髄炎/慢性疲労症候群 (ME/CFS) の原因および潜在的なマーカーの一つであることを画像解析から報告し(2020, Fujii)、自律神経受容体に対する自己抗体に関連した脳内構造ネットワーク異常を明らかにしました。治療の観点から、この自己抗体を除去する、あるいは産生を減少させる治療法が抗体価の高い患者に有効な可能性を指摘しました。(2020, Satake)
リツキシマブ(Rituximab)は、抗ヒトCD20(ヒトCD20はヒトリンパ球B細胞のみに発現し、正常・腫瘍細胞は問わず、preB~成熟B細胞にかけて細胞膜表面に認められるB細胞表面分子)ヒト・マウスキメラ抗体からなるモノクローナル抗体であり、抗体を産生するB細胞を枯渇させる作用を持ち、B細胞枯渇剤とも呼ばれます。自己抗体が問題となる自己免疫疾患への有効性が期待されている薬剤ですが、現時点でのME/CFSに対する有効性はまだ結論が出ていません。(2015, Fluge)(2019, Fluge)
ME/CFS対する薬剤の総論も出ていますが結論は出ていません。免疫調整剤としてのステロイド、リンタトリモド(2016, Mittichel)なども有意な結果は出ていません。(2021, Toogood)
ME/CFSに対するこれまでに実施された薬理的および非薬理的RCTの総論においても結論は出ていません。(2020, Kim)
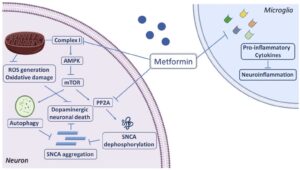
ME/CFSに対して、ミトコンドリアでのグルコース代謝を最適化する治療の重要性が指摘されています。具体的には、メトホルミン、またはメルドニウムを含むインスリン抵抗性を修正するモモルディカ・チャランティア抽出物で治療することによって、ミトコンドリアへのグルコースの輸送を改善します。ジクロロ酢酸ナトリウムがピルビン酸デヒドロゲナーゼを活性化します。コエンザイムQ10などの栄養サポートによって、酸化および炎症障害を軽減します。(2020, Comhaire)
ME/CFS 患者の細胞では AMPK の障害があり(2015, Brown)、in vitroでは、メトホルミンを使用した AMPK の活性化により、線維筋痛症患者由来の線維芽細胞の生体エネルギープロファイルが改善されること(2015, Alcocer-Gómez)、ME/CFS患者由来の培養ヒト骨格筋細胞におけるAMPKの活性化とグルコースの取り込みを増加させること(2018, Brown)が報告されています。
ME/CFS 患者の酸化ストレスの増加を軽減するための抗酸化サプリメントとしてメラトニン(1mg)と亜鉛(10mg)の投与の有効性が報告されています。(2021, Castro-Marrero)
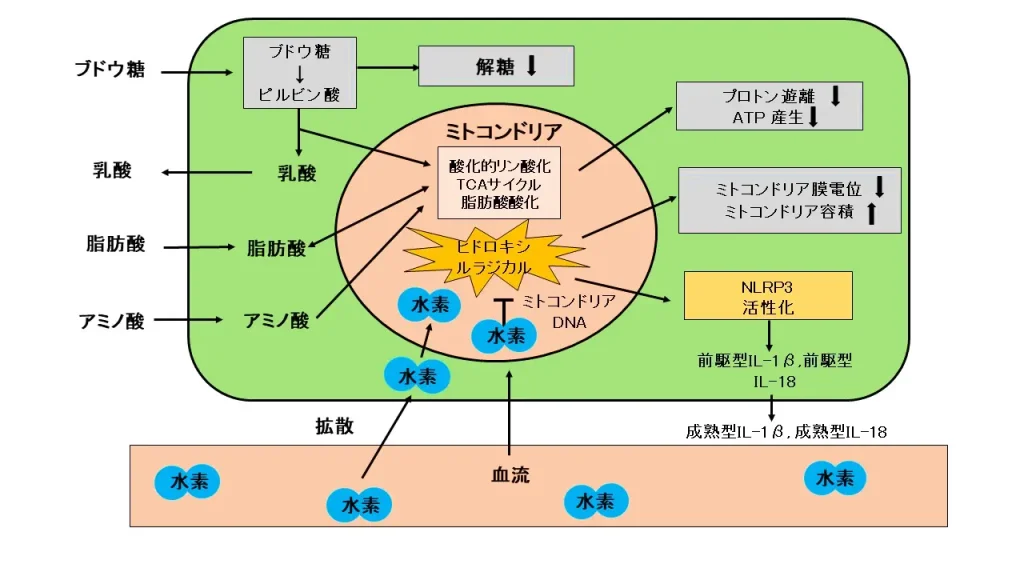
文献レビューでは、水素ガスがME/CFSの酸化ストレスに対する治療として有効である可能性があることが示唆されています。(2022, Hirano)
ME/CFSの疲労症状に対してオゾン療法が有効であることが報告されています。(2022, Tirelli)
ME/CFS で古典的に研究されている炎症と免疫機能障害は、機能不全のエネルギー論、腸の健康、または自律神経と副腎の調節不全と絡み合っている可能性があります。代謝およびミトコンドリア機能障害の証拠は、非効率的な呼吸、TCA サイクル基質の供給障害、および代替代謝産物の利用への代謝シフトを示しています。免疫エフェクター細胞の機能不全、慢性炎症、シグナル伝達の欠陥、および酸化ストレスの上昇は、機能不全のエネルギー論だけでなく、異常な腸の生理機能および微生物叢の組成とも相互作用する可能性があります。腸へのこれらの影響は、ミトコンドリア機能にも関係している可能性があり、逆もまた同様です。(2019, Missailidis)
キヌレニン経路は、筋痛性脳脊髄炎/慢性疲労症候群 (ME/CFS) の複雑なパズルの重要な欠けているピースであると指摘されています。(2022, Kavyani)
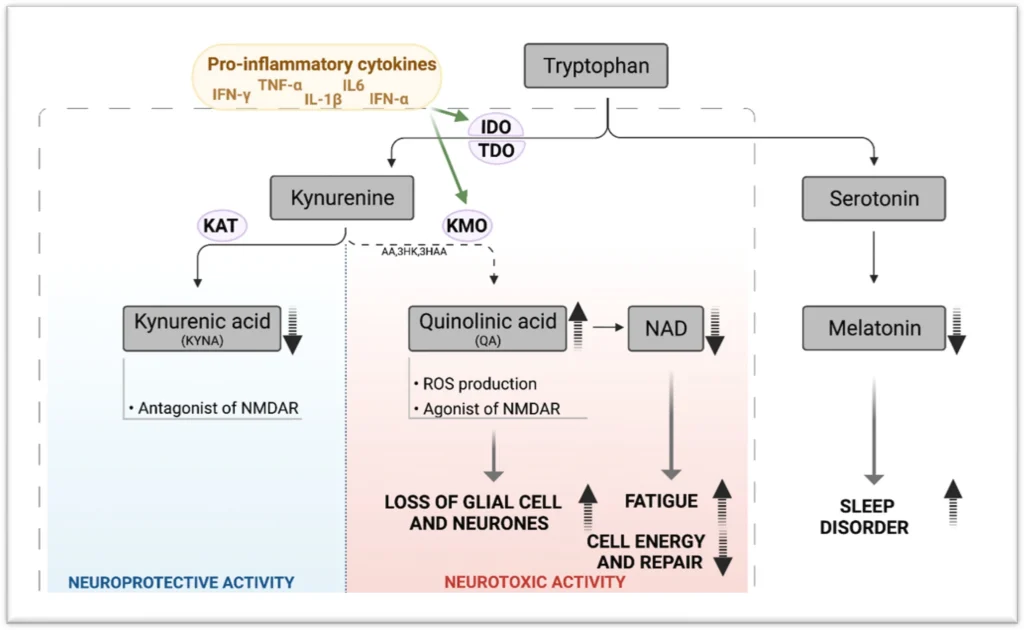
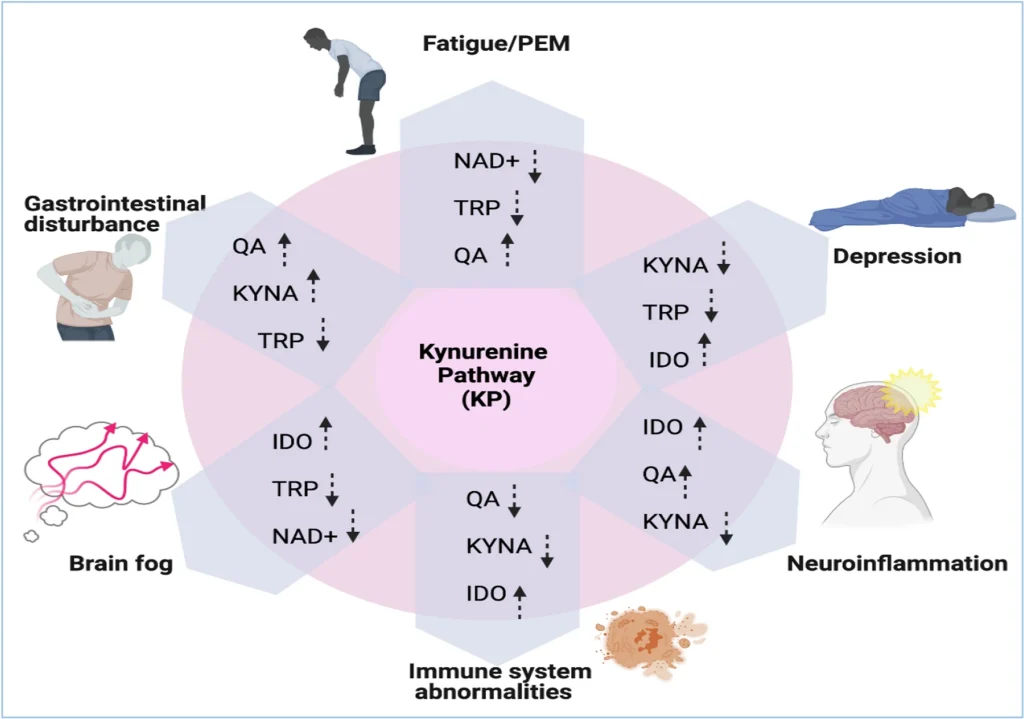
セロトニン経路とキヌレイン経路を切り替えるIDO代謝トラップがME/CFSの原因であると提唱されています。(2019, Kashi)
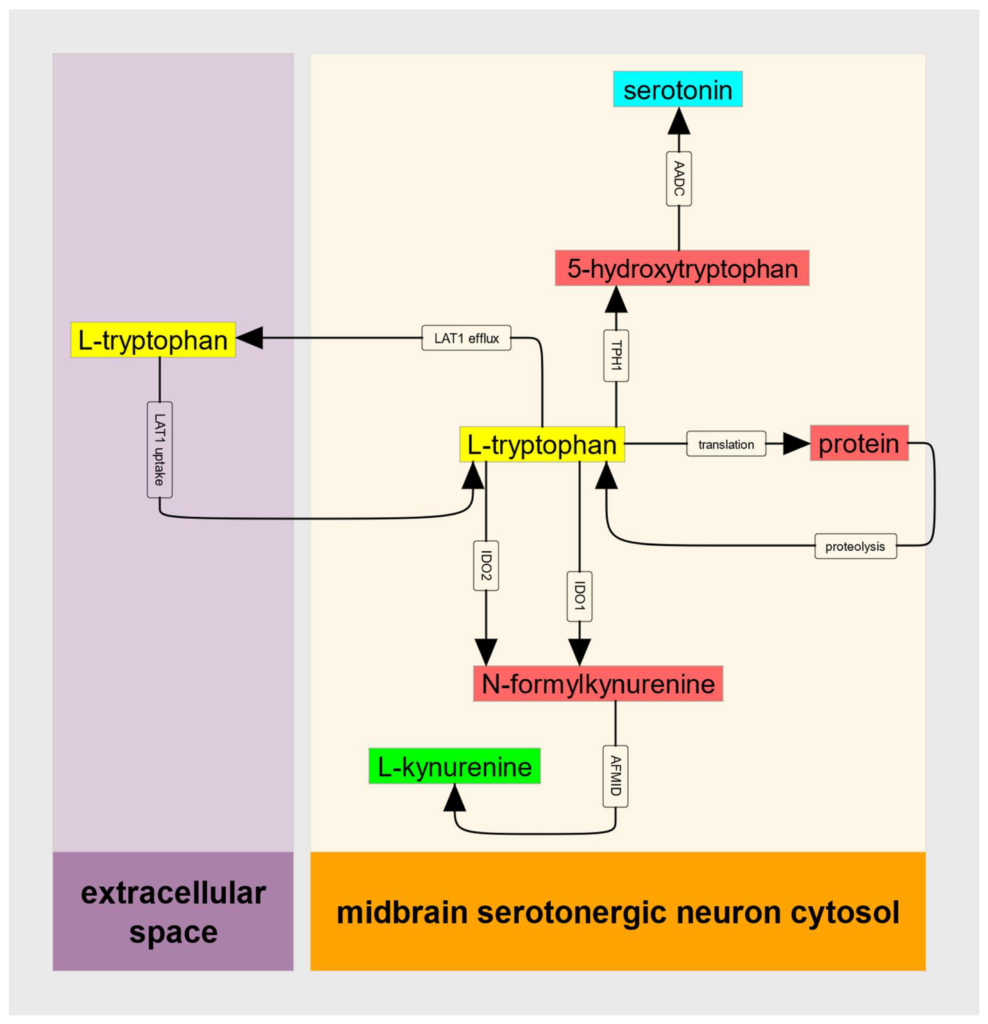
酸化還元(レドックス)の不均衡によってME/CFSが発症に関連することが総括されています。(2021, Paul)
ME/CFS の特徴であるミトコンドリア機能障害と自己免疫の要素がウイルス感染に起因する可能性が指摘されています。(2018, Rasa)
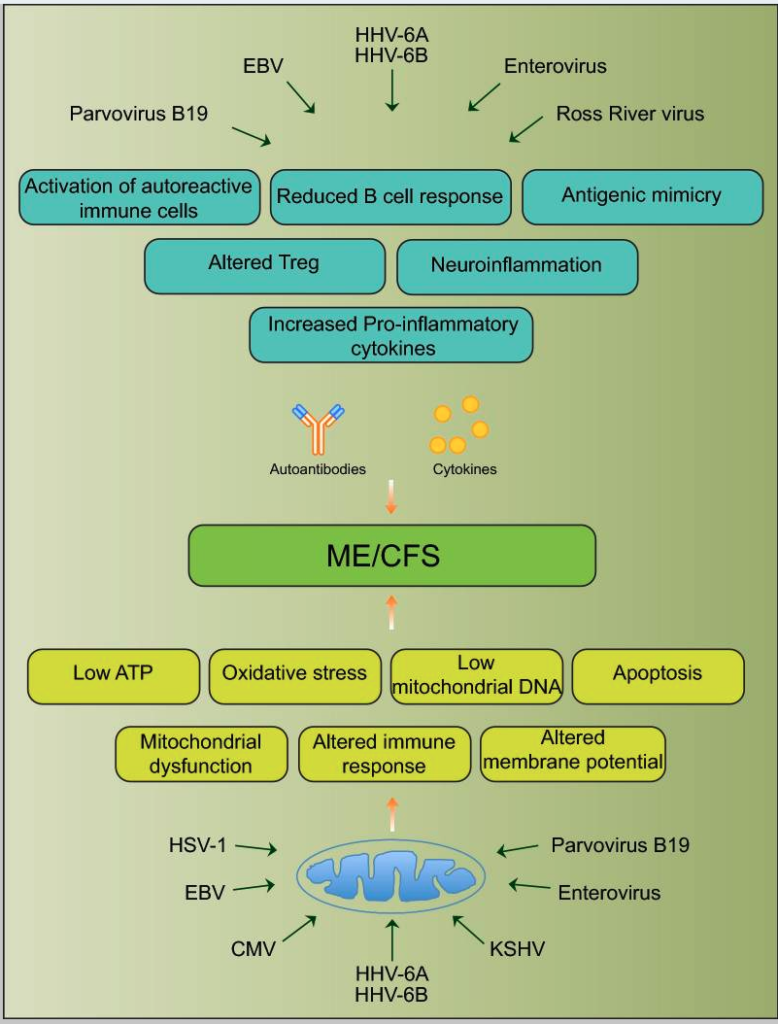
HPVワクチン後遺症によるME/CFSでは、分子模倣を介して様々なヒトタンパク質に対して自己免疫反応を引き起こす可能性が指摘されています。(2020, Phelan)