新型コロナ mRNAワクチンによるミトコンドリアの脆弱性が心筋炎の根底にある
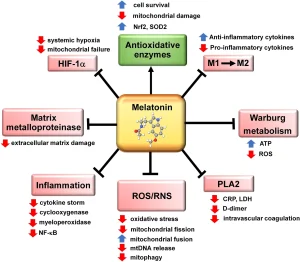
SARS‐CoV‐2に対するmRNAワクチンは、COVID-19パンデミックに対抗するために広く採用されています。しかし、心筋炎は稀ではありますが重篤な副作用として顕在化し、主に若年男性に見られます。ここでは、ミトコンドリアの脆弱性がmRNAワクチン関連心筋炎と関連していることを示します。我々の症例対照研究では、ワクチン接種後の心筋炎患者はミトコンドリアの異常を示しました。ミトコンドリア損傷の影響を検証するため、mRNAワクチンはポリグ+/D257Aマウスに投与されました。このマウスはヘテロ接合的に校正欠損のミトコンドリアDNAポリメラーゼを発現させ、ミトコンドリアをストレスに感作します。Polg+/D257AマウスにおけるmRNAワクチン接種は左心室駆出率を低下させ、心筋免疫細胞の浸潤を誘導しました。バゼドキシフェンは、選択的エストロゲン受容体モジュレーターであり、Polg+/D257Aマウスにおける心機能の低下を防止し、エストロゲンシグナル伝達に対する保護的役割を示唆した。特に、mRNAワクチン接種はミトコンドリアの活性酸素種を誘導し、心筋細胞においてネクロプトーシス関連キナーゼであるRIPK3の活性化をもたらした。総じて、我々はミトコンドリアの脆弱性がmRNAワクチン接種後の心筋炎の潜在的リスク因子であり、活性酸素種が媒介するネクロプトーシスシグナル伝達による可能性があると提案します。
【まとめ】
mRNAワクチン接種 → 【第一相】LNP脂質 → ミトコンドリアROS → ネクロプトーシス →(心臓自己抗原放出・局所炎症環境形成)
【第二相】分子模倣 → T細胞性自己免疫 → 持続的局所炎症
→ 全接種者において程度の差はあれ普遍的に生じ 少なくとも180日間持続する心筋への不可逆的損傷
→ コロナ感染による心筋への二次的免疫攻撃
未接種感染による心筋炎リスクは 重症化患者に実質限定されるため mRNAワクチン投与の リスク・ベネフィット計算が根本から問い直される必要がある。