メラトニンの大量療法
まとめ:メラトニンの大量療法では、最大で1日300mg(経口または座薬)までの報告があるが、副作用はほとんど報告されていません。
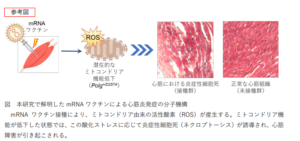
メラトニンの神経保護化合物および抗酸化物質としての可能性を、(1)培養運動ニューロン細胞(NSC-34)、(2)ALSの遺伝子改変マウスモデル(SOD1 G93Aトランスジェニックマウス)、および(3)孤発性ALS患者31名のグループで検討した。その結果、メラトニンは培養運動ニューロンのグルタミン酸誘発性細胞死を軽減することがわかった。SOD1 G93Aトランスジェニックマウスでは、高用量の経口メラトニンが疾患進行を遅らせ、生存期間を延長した。臨床安全性試験において、高用量(300mg/日)の直腸メラトニンを最長2年間投与したところ、忍容性は良好でした。重要なことに、酸化ストレスの代替マーカーとなる血清タンパク質カルボニル濃度はALS患者で上昇していましたが、メラトニン投与により対照群の値まで正常化しました。前臨床における有効性とヒトにおける安全性の実証というこの組み合わせは、高用量メラトニンがALSにおける抗酸化作用を介した神経保護を目的とした臨床試験に適していることを示唆しています。(2006, Weishaupt)
本研究では16件の論文を対象とし、そのうち9件はランダム化比較試験(RCT)であった。被験者の平均年齢は55.3歳から77.6歳までであった。メラトニンの投与量は0.1mgから50mg/kgまでで、全研究で経口投与された。介入前後のメラトニン濃度を比較したところ、介入後のメラトニン濃度は用量依存的に有意に上昇したことが明らかになった。血清および尿中の最大濃度はプラセボと比較して全て上昇しており、高齢者では若年者よりも上昇幅が大きいことが示された。血清および尿中の最大濃度に達するまでの時間に差はなかったものの、高用量のメラトニン濃度は低用量よりも一定の閾値を超える状態がより長く維持された。(2014, Vural)
30歳以上の成人を対象に高用量メラトニン(10mg以上)を調査したランダム化比較試験を対象としました。2名の研究者がPRISMAガイドラインに従って独立して論文を抽出しました。バイアスのリスクは、3名の研究者からなる委員会によって評価されました。合計3861名の参加者を含む79件の研究が特定されました。研究には、幅広い疾患が含まれていました。メタアナリシスは、ランダム効果モデルを使用してデータを統合しました。検討されたアウトカムは、有害事象(AE)、重篤な有害事象(SAE)、およびAEによる中止の数でした。合計29の研究(37%)では、AEの有無について言及されていませんでした。全体として、メタアナリシスの事前規定されたバイアスリスクの低い基準を満たした研究はわずか4件でした。その小さなサブセットでは、メラトニンはSAE(発生率比 = 0.88 [0.52, 1.50]、p = .64)またはAEによる中止(0.93 [0.24, 3.56]、p = .92)の検出可能な増加を引き起こしませんでしたが、眠気、頭痛、めまいなどのAEのリスクを高めるようでした(1.40 [1.15, 1.69]、p < .001)。全体として、高用量メラトニン研究からのAE報告は限られています。この限られた証拠に基づくと、メラトニンは良好な安全性プロファイルを持っているように思われる。(2021, Schrire)
37件のRCTが選択基準を満たしました。メラトニンの1日投与量は0.15mgから12mgまででした。被験者は最長29週間モニタリングされましたが、ほとんどの研究ははるかに短い期間(4週間以下)でした。最も頻繁に報告された有害事象は、日中の眠気(1.66%)、頭痛(0.74%)、その他の睡眠関連の有害事象(0.74%)、めまい(0.74%)、低体温(0.62%)でした。重篤または臨床的に重要な有害事象はごくわずかしか報告されていませんでした。これらには、興奮、疲労、気分の変動、悪夢、皮膚刺激、動悸が含まれます。ほとんどの有害事象は、メラトニンの調整なしに数日以内に自然に解消するか、治療の中止後すぐに解消しました。メラトニンは一般的に安全で忍容性が高いと考えられました。(2019, Besag)